中国薬事申請事情:医薬品包装・医薬品添加物のやり方が変わりました
中国薬事申請事情:医薬品包装・医薬品添加物のやり方が変わりました
NMPAの医薬品に関する承認審査を簡素化し、医薬品登録制度を整備することを目的に、2017年に改定が行われました。(国家食品監督管理総局 2017-42号)
最近医薬品包装・医薬品添加物のメーカーは、製薬企業に登記番号を求められるケースが多く、製品の登記が求められるようになった。
アメリカのDMF制度や日本の原薬登記簿と類似した制度になります。
尚、アメリカと日本は任意登記と異なり、中国側では極力推薦となっています(必須まではまだ至っていない)。
対象となるのは…
a. 医薬品包装(中国語:薬包材)
医薬品の生産または処方の際に、医薬品と直接接触する包装材料、または容器を指す。
b. 医薬品添加物(中国語:薬用補料)
医薬品の生産または処方の際に使われる添加剤などを指し、医薬品の活性成分を除き、安全性において合理的に評価され、かつ医薬品製剤の成分に含まれる物質を指す。
改定の内容は…
a. 医薬品包装・医薬品添加物の概念を明確化し、既存の医薬品製剤や医療器から切り離し、単独の登記制度にて運用する。
b. 医薬品登録申請(主体となる医薬品の申請)の時に、医薬品と一緒に承認審査を行う。
この際、すでに登記済みの医薬品包装、医薬品添加物は、主体となる医薬品との関連審査(主にマッチングを確認する)を行うことになる。
改定の結果…
医薬品包装・医薬品添加物の製販企業にとって、かなりの時間とコストの節約となります。
例1. 時間の短縮
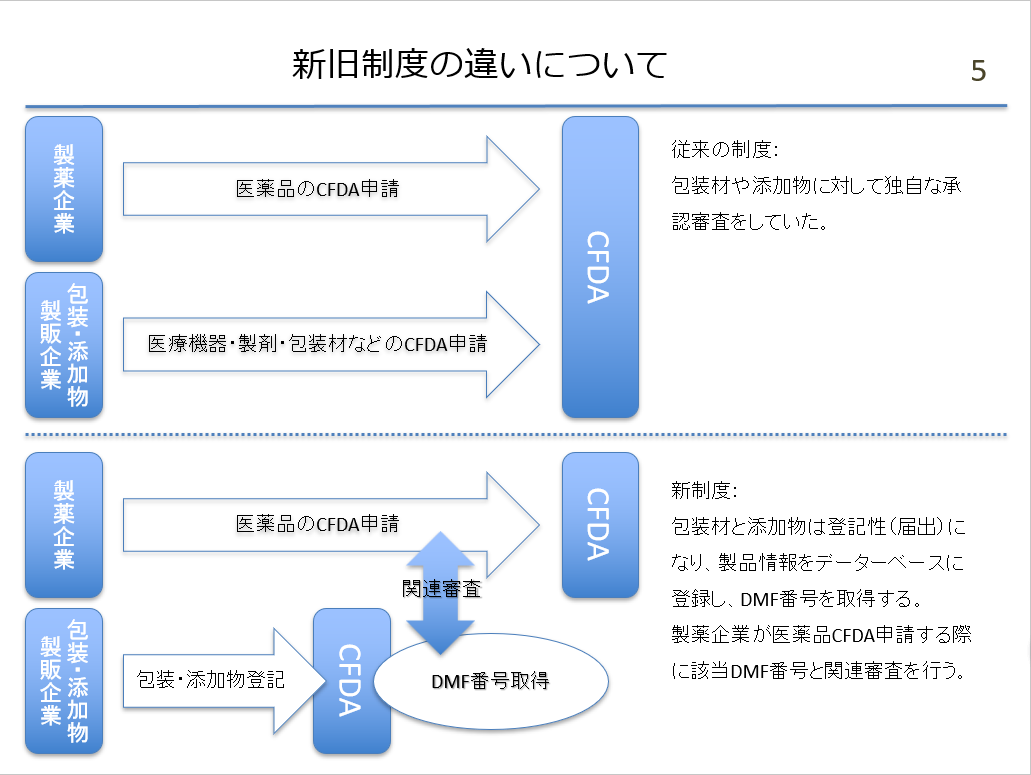
▼ 資料整備完了後、NMPAへ正式提出から審査完了までの所要時間
従来:約3カ月 ⇒ 現在:約10~20営業日
例2. 一部の医療機器が包装に再分類によるコスト削減
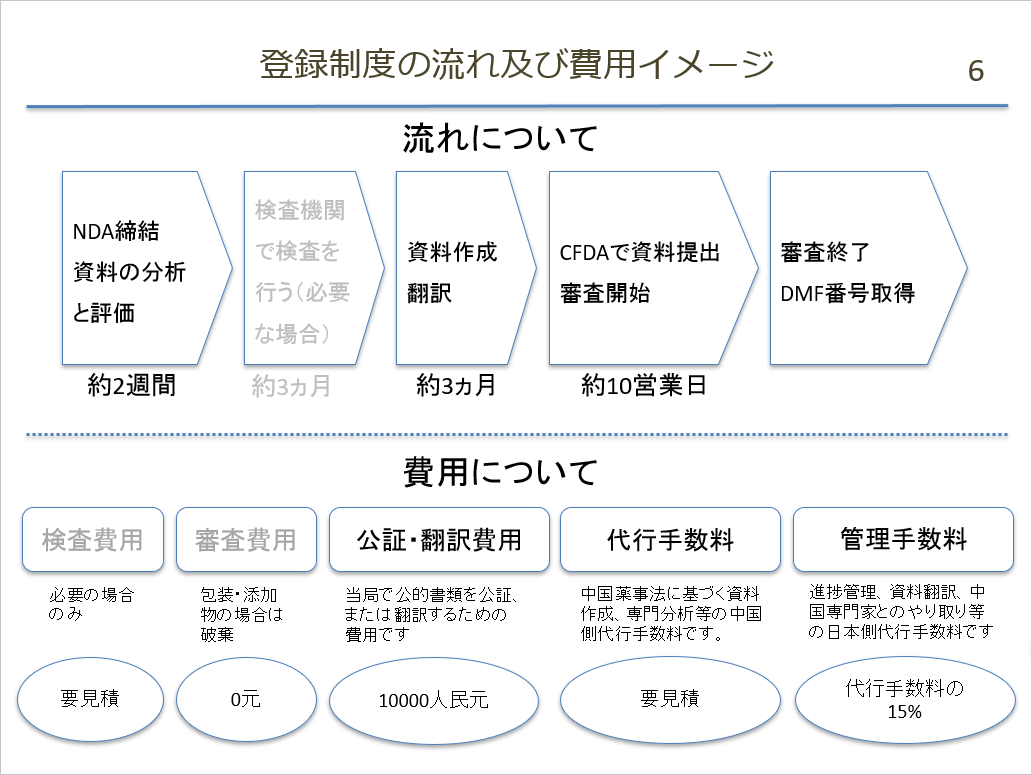
▼ 注射器、注射シリンジ、注射針を例とする審査費用:即ちNMPA審査を行うための料金
旧制度だと医療機器 ———— 審査費用24万元
新制度だと医薬品包装 ——— 審査費用0元
a. 最低でも1製品つき約400万円の削減となります。
b. 製品により、検査機関での検査が必要な場合があります。
c. 申請では従来通り中国薬事法に基づいて、専門スタッフが製品データの分析、検討を行い申請資料を作成することになるため、製品により代行費用が大幅に上下します。(要見積り)
医薬品包装・医薬品添加物の中国登記は弊社にお任せください
弊社は中国現地の薬事申請会社と連携しており、貴社の製品登記をコーディネートさせていただきます。